
Perché ti sei ammalato? Le 7 Cause Reali dell'Insulino Resistenza (Non è solo lo zucchero)
"Dottore, è colpa dello zucchero?" "Smetta di mangiare pane e pasta e dimagrirà." "Ha l'insulina alta perché non ha forza di volontà."
Quante volte hai sentito queste frasi? Il problema è che sono troppo semplici. E, in parte, sbagliate.
Non fraintendermi: i carboidrati raffinati giocano un ruolo cruciale. Ma se l'insulino resistenza fosse causata solo dallo zucchero, come spiegheresti che intere popolazioni asiatiche mangiano l'80% di carboidrati (riso) e restano magre? O che ci sono persone in low carb rigorosa che possono comunque essere resistenti all'insulina?
La verità è che l'insulino resistenza è un effetto domino. È il risultato di una tempesta perfetta innescata da decine di cause che si amplificano a vicenda. In questo dossier tecnico analizziamo le 7 categorie di cause che hanno portato il tuo corpo a sviluppare insulino resistenza. Alcune puoi cambiarle. Altre no. Ma conoscerle è l'unico modo per comprendere dove intervenire.
La Causa Paradossale: L'Insulina Stessa
 Iniziamo con il paradosso più grande della medicina metabolica: la causa principale dell'insulino resistenza è l'insulina stessa.
Iniziamo con il paradosso più grande della medicina metabolica: la causa principale dell'insulino resistenza è l'insulina stessa.
Sembra assurdo, vero? Come può l'ormone che deve curare il problema, essere il problema? Pensa a cosa succede nella vita di tutti i giorni:
- Se prendi troppi antibiotici → I batteri diventano resistenti.
- Se bevi caffè ogni ora → Sviluppi tolleranza (non ti fa più effetto).
- Se urli continuamente a qualcuno → Quella persona smette di ascoltarti.
Il Meccanismo dell'Adattamento Cellulare Le tue cellule fanno la stessa cosa. Quando sono esposte costantemente a livelli alti di insulina (iperinsulinemia), si proteggono "tappandosi le orecchie".
- Downregulation: Riducono il numero di recettori (le "porte" per il glucosio).
- Alterazione della cascata di segnalazione: Anche i recettori ancora presenti diventano meno sensibili, bloccando il segnale interno che dovrebbe attivare il GLUT4 (il trasportatore di glucosio).
È un circolo vizioso mortale: Mangi spesso → L'insulina sale → Le cellule si difendono e diventano resistenti → Il pancreas deve urlare più forte (produrre più insulina) per farsi sentire → La resistenza peggiora. Ecco perché abbassare l'insulina è la terapia fondamentale: dobbiamo smettere di urlare alle cellule.
Cosa innesca l’iperinsulinemia iniziale?
Questa è la domanda da un milione di dollari. Se l'insulina alta causa resistenza, cosa causa l'insulina alta iniziale?
La risposta: tutte le altre cause che stiamo per esplorare. Dieta, stress, infiammazione, obesità, sedentarietà, tossine ambientali – ognuna di queste può essere la scintilla che innesca il circolo vizioso.
Ma una volta che l'iperinsulinemia cronica si stabilisce, diventa essa stessa il motore principale della malattia, indipendentemente dalla causa iniziale.
Questo è il motivo per cui abbassare l'insulina è la strategia terapeutica fondamentale!
CAUSA 1: Ormoni Antagonisti (La guerra interna)
Il tuo corpo è un ecosistema. L'insulina non lavora da sola, ma combatte contro altri ormoni "antagonisti" che vogliono mantenere lo zucchero alto nel sangue per darti energia immediata. Quando questi ormoni sono sempre attivi, l'insulina perde la battaglia.
Cortisolo: Lo Stress Cronico
Il cortisolo è l'ormone dello stress. È utile se devi scappare da un leone, ma è devastante se è alto tutto il giorno a causa di:
- Privazione cronica del sonno
- Sovrallenamento sportivo senza recupero
- Infiammazione cronica
- Restrizione calorica estrema prolungata
- Farmaci cortisonici (prednisone, cortisone), usati per asma, artrite, malattie autoimmuni
Come induce insulino resistenza?
- Stimola la gluconeogenesi epatica: Ordina al fegato di produrre glucosio anche quando non ne hai bisogno, aumentando la glicemia basale.
- Blocca l'uptake di glucosio nei muscoli: Rende le cellule muscolari resistenti all'insulina per "risparmiare" glucosio per il cervello durante lo stress.
- Promuove la lipolisi e lipotossicità: Mobilita acidi grassi liberi dal tessuto adiposo, che si accumulano nel fegato e nei muscoli causando resistenza (via ceramidi – vedi sotto).
- Aumenta il grasso viscerale: Il cortisolo alto promuove l'accumulo di grasso addominale, il più insulino-resistente.
Se vivi in uno stato di stress cronico, sei programmato per diventare insulino-resistente, indipendentemente dalla tua dieta.
Adrenalina: Lo sprint infinito
È l'ormone della lotta o fuga. Basta una piccola scarica di adrenalina per ridurre la sensibilità all'insulina del 40% in pochi minuti.
Come agisce:
- Attiva la glicogenolisi (rilascio di glucosio dal fegato)
- Blocca la secrezione di insulina dal pancreas
- Rende i muscoli temporaneamente resistenti
In condizioni normali, l'adrenalina sale per minuti (corri da un pericolo, poi ti calmi). Ma se vivi in uno stato di attivazione simpatica costante – ansia cronica, ipervigilanza, consumo eccessivo di caffeina, mancanza di sonno, mantieni l'adrenalina cronicamente elevata.
Ormoni Tiroidei: La Tiroide ‘’Lenta’’
L'ipotiroidismo (tiroide che funziona poco) è strettamente legato all'insulino-resistenza attraverso due meccanismi:
- Riduzione dei recettori insulinici: Gli ormoni tiroidei (T3, T4) regolano l'espressione dei recettori dell'insulina sulle cellule. Quando la tiroide è lenta, ci sono meno recettori disponibili.
- Rallentamento metabolico: Il metabolismo basale diminuisce, riducendo l'uptake di glucosio da parte dei tessuti.
Molte donne con PCOS, ad esempio, hanno contemporaneamente insulino-resistenza e ipotiroidismo subclinico: le due condizioni si alimentano a vicenda.
Ormoni Sessuali: Menopausa e Andropausa
Estrogeni (nelle donne) e testosterone (negli uomini e donne) hanno un effetto protettivo contro l'insulino-resistenza.
Cosa succede quando calano:
- Menopausa (donne): La perdita di estrogeni è associata a:
- Aumento del grasso viscerale
- Riduzione della sensibilità insulinica
- Aumento del rischio cardiovascolare e diabete tipo 2
- Andropausa (uomini): Il calo di testosterone causa:
- Perdita di massa muscolare (meno "lavandini" per il glucosio)
- Aumento del grasso addominale
- Peggioramento della sensibilità insulinica
Questo spiega perché l'incidenza di insulino-resistenza e diabete aumenta drasticamente dopo i 50 anni.
CAUSA 2: Obesità (Ma Non Come Pensi)
"Sei insulino-resistente perché sei grasso."
Questa frase viene detta milioni di volte ogni giorno. Ed è parzialmente vera, l'obesità è fortemente correlata all'insulino-resistenza. Ma il meccanismo non è "hai troppo grasso, quindi sei resistente". È molto più complesso.
Non è quanto grasso hai. È dove è il grasso, come è distribuito, e quanto sono grandi le cellule adipose.
Ipertrofia vs Iperplasia: La Dimensione Conta
Questo è il concetto più importante che nessuno ti spiega.
Quando aumenti di peso, il grasso può espandersi in due modi:
- Iperplasia (Espansione Sana, ma limitata all’età puberale, fin quando le ricerche non la smentiscono)
- Le cellule adipose si moltiplicano in numero
- Rimangono piccole e sensibili all'insulina
- Il grasso viene immagazzinato in modo sicuro nel tessuto adiposo sottocutaneo
- Risultato: Puoi essere sovrappeso ma metabolicamente sano
- Ipertrofia (Espansione Patologica)
- Le cellule adipose crescono in dimensione (si gonfiano)
- Diventano enormi, sature, disfunzionali
- Risultato: Insulino-resistenza, infiammazione, lipotoxicità
Perché le cellule ipertrofiche sono insulino-resistenti?
- Perdita di sensibilità: Una cellula adiposa troppo grande smette di rispondere all'insulina. Normalmente, l'insulina segnala: "Smetti di rilasciare grassi" (blocco della lipolisi). Ma una cellula ipertrofica ignora questo segnale.
- Lipolisi incontrollata: Inizia a "perdere" continuamente acidi grassi liberi nel sangue, che viaggiano verso fegato e muscoli.
- Infiammazione: Le cellule grasse giganti rilasciano citochine pro-infiammatorie (TNF-α, IL-6) che causano resistenza sistemica.
- Produzione di ceramidi: Quando gli acidi grassi si accumulano in fegato e muscoli, vengono convertiti in ceramidi, grassi tossici che bloccano fisicamente la segnalazione dell'insulina (vedi sotto).
Cosa Causa Ipertrofia Adipocitaria?
Due molecole specifiche forzano le cellule adipose a crescere in dimensione anziché in numero:
- 4-HNE (4-Idrossinonenale)
Questa molecola deriva dall'ossidazione degli acidi grassi omega-6 (acido linoleico), abbondanti negli oli vegetali industriali (mais, girasole, soia, canola).
- Quando consumi oli vegetali ricchi di omega-6, questi si integrano nelle membrane cellulari
- L'ossidazione (stress ossidativo, radicali liberi) trasforma gli omega-6 in 4-HNE
- Il 4-HNE costringe le cellule adipose a diventare ipertrofiche anziché moltiplicarsi
- Risultato: cellule grasse giganti e resistenti
- C1P (Ceramide-1-Fosfato)
Deriva dall'infiammazione cronica. Le citochine infiammatorie producono C1P, che blocca la proliferazione degli adipociti forzandoli a espandersi in dimensione.
Conclusione: Non è la quantità totale di grasso il problema primario, è il fatto che quel grasso è intrappolato in cellule giganti, disfunzionali e infiammate.
Grasso Viscerale vs Sottocutaneo: La Posizione È Tutto
Due persone con lo stesso peso e BMI possono avere rischi metabolici completamente diversi a seconda di dove si accumula il grasso.
Grasso Sottocutaneo (Fianchi, Cosce, Glutei)
- Metabolicamente relativamente innocuo
- Immagazzina energia in modo sicuro
- Produce adiponectina (ormone che migliora la sensibilità insulinica)
- Tipico del fenotipo "pera" (più comune nelle donne pre-menopausa)
Grasso Viscerale (Addome, Intorno agli Organi)
- Metabolicamente estremamente pericoloso
- Produce citochine infiammatorie (TNF-α, IL-6, resistina)
- Rilascia acidi grassi liberi direttamente nel sistema portale epatico (verso il fegato)
- Causa steatosi epatica (fegato grasso)
- Tipico del fenotipo "mela" (più comune negli uomini e donne post-menopausa)
Perché il grasso viscerale è così dannoso?
Il grasso viscerale è più metabolicamente attivo e infiammatorio del grasso sottocutaneo. È letteralmente un organo endocrino che riversa ormoni e grassi direttamente nel fegato, il centro di comando metabolico del corpo.
Questo è il motivo per cui la circonferenza vita è un predittore di insulino-resistenza molto migliore del BMI:
- 102 cm (uomini) o >88 cm (donne) = alto rischio metabolico
Puoi avere BMI normale ma circonferenza vita alta (fenotipo TOFI – "Thin Outside, Fat Inside") e essere gravemente insulino-resistente.
Grasso Ectopico: Il Grasso Dove Non Dovrebbe Stare
Quando le cellule adipose sono piene (sature), il grasso inizia a depositarsi dove non dovrebbe mai stare:
- Fegato → Steatosi epatica non alcolica (NAFLD)
- Muscoli → Lipidi intramiocellulari
- Pancreas → Disfunzione beta-cellulare
- Cuore → Cardiomiopatia
In questi tessuti, i grassi vengono convertiti in ceramidi, molecole lipidiche tossiche che interferiscono direttamente con la segnalazione dell'insulina.
Ceramidi: I Killer Metabolici
Le ceramidi sono il meccanismo finale comune attraverso cui il grasso ectopico causa insulino-resistenza.
Come agiscono:
- Bloccano la cascata di segnalazione dell'insulina (interferiscono con AKT, una proteina chiave)
- Impediscono la traslocazione del GLUT4 alla membrana cellulare
- Inducono apoptosi (morte cellulare) nelle cellule beta del pancreas
Cosa produce ceramidi:
- Acidi grassi saturi in eccesso (specialmente acido palmitico)
- Infiammazione cronica
- Stress ossidativo
- Accumulo di grasso ectopico in fegato/muscoli
Le ceramidi sono così importanti che alcuni ricercatori le considerano il marker più accurato di insulino-resistenza, più dell'insulina stessa.
CAUSA 3: Infiammazione Cronica
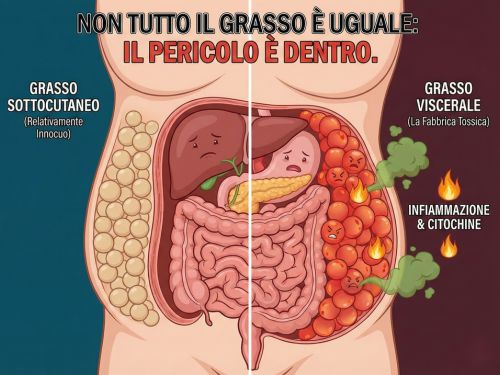 L'insulino-resistenza è spesso descritta come uno stato infiammatorio cronico di basso grado. Il sistema immunitario e il metabolismo sono profondamente intrecciati, quando uno si altera, trascina l'altro con sé.
L'insulino-resistenza è spesso descritta come uno stato infiammatorio cronico di basso grado. Il sistema immunitario e il metabolismo sono profondamente intrecciati, quando uno si altera, trascina l'altro con sé.
Infiammazione → Insulino-Resistenza:
- Le citochine pro-infiammatorie (TNF-α, IL-6, IL-1β) attivano vie di segnalazione (come JNK e IKK) che fosforilano i substrati del recettore dell'insulina, bloccando il segnale
- L'infiammazione promuove la conversione di acidi grassi in ceramidi tossiche
- Le specie reattive dell'ossigeno (ROS) danneggiano le proteine della cascata insulinica
Insulino-Resistenza → Infiammazione:
- L'iperinsulinemia attiva NF-κB, un fattore di trascrizione pro-infiammatorio
- Il glucosio alto (glicazione) produce AGEs (Advanced Glycation End-products) che attivano recettori infiammatori
- Le cellule adipose ipertrofiche rilasciano citochine infiammatorie
È un altro circolo vizioso: più sei infiammato, più diventi resistente. Più sei resistente, più ti infiammi.
Fonti di Infiammazione Cronica
- Obesità Viscerale
Come abbiamo visto, il grasso viscerale è una fabbrica di citochine infiammatorie. Più grasso addominale hai, più infiammazione produci.
- Malattie Autoimmuni e Infiammatorie
Condizioni come:
- Artrite reumatoide
- Lupus eritematoso sistemico
- Psoriasi
- Malattie infiammatorie intestinali (Crohn, colite ulcerosa)
Sono tutte fortemente associate a insulino-resistenza. L'infiammazione sistemica causata da queste malattie induce resistenza anche in assenza di obesità.
- Infezioni Croniche
Infezioni virali o batteriche persistenti (es. epatite C, HIV, parodontite cronica) mantengono il sistema immunitario attivato, producendo citochine infiammatorie.
- Intestino Permeabile (Leaky Gut)
Quando la barriera intestinale è compromessa, tossine batteriche chiamate lipopolisaccaridi (LPS) possono "leaky" nel sangue.
- Gli LPS sono riconosciuti come minacce dal sistema immunitario
- Scatenano una risposta infiammatoria sistemica
- Inducono insulino-resistenza attraverso l'attivazione di TLR4 (Toll-Like Receptor 4)
Cosa causa leaky gut?
- Dieta ricca di zuccheri e grassi processati
- Antibiotici (distruggono il microbioma)
- Alcol
- Stress cronico
- FANS (antinfiammatori non steroidei) usati cronicamente
- Stress Ossidativo
Le specie reattive dell'ossigeno (ROS) danneggiano proteine, lipidi e DNA. Quando i ROS superano le difese antiossidanti del corpo, causano:
- Danneggiamento dei recettori dell'insulina
- Produzione di molecole infiammatorie (4-HNE dalle membrane lipidiche)
- Disfunzione mitocondriale (le centrali energetiche producono ancora più ROS)
Fonti di stress ossidativo:
- Dieta ricca di grassi ossidati (oli vegetali riscaldati, fritti)
- Fumo
- Inquinamento atmosferico
- Esercizio eccessivo senza recupero
- Radiazioni (UV, raggi X)
CAUSA 4: Fattori Ambientali e Tossine (Cosa Respiri e Assorbi)
Il tuo ambiente è un fattore determinante per la tua salute metabolica. Anche con dieta e stile di vita perfetti, l'esposizione cronica a tossine ambientali può indurti insulino-resistenza.
Inquinamento Atmosferico
L'esposizione al particolato fine (PM2.5), le particelle microscopiche presenti nell'aria inquinata, è un fattore di rischio indipendente per insulino-resistenza e diabete tipo 2.
Meccanismo:
- Le particelle ultrafini vengono inalate e assorbite nel sangue
- Causano infiammazione sistemica
- Inducono stress ossidativo
- Alterano la funzione mitocondriale
Dati epidemiologici:
- Ogni aumento di 10 µg/m³ di PM2.5 è associato a un aumento del 25% del rischio di diabete tipo 2
- Le popolazioni che vivono vicino a strade trafficate hanno tassi più alti di insulino-resistenza
Non puoi controllare l'aria che respiri, ma vivere in aree urbane altamente inquinate è un fattore di rischio silenzioso.
Fumo di Sigaretta
Il fumo è devastante per la sensibilità insulinica attraverso tre meccanismi:
- Nicotina: Agisce direttamente sulle cellule adipose, inducendo resistenza e lipolisi incontrollata
- Infiammazione: Il fumo attiva una risposta infiammatoria cronica nei polmoni e sistemica
- Stress ossidativo: Produce enormi quantità di radicali liberi
Importante: Anche il fumo passivo e il fumo di terza mano (residui di fumo su vestiti e superfici) hanno effetti misurabili sulla sensibilità insulinica, specialmente nei bambini.
Tossine Alimentari e Contaminanti
BPA (Bisfenolo A) – Plastiche
Il BPA è un interferente endocrino presente in:
- Bottiglie di plastica
- Rivestimenti interni di lattine
- Scontrini termici
- Contenitori alimentari in plastica
Meccanismo:
- Imita gli estrogeni (xenoestrogeno)
- Altera la funzione delle cellule beta pancreatiche
- Induce insulino-resistenza nei tessuti periferici
Pesticidi
I pesticidi organofosforati e organoclorurati si accumulano nel tessuto adiposo e sono predittori significativi del rischio di diabete.
- Interferiscono con la segnalazione insulinica
- Danneggiano i mitocondri
- Causano stress ossidativo
MSG (Glutammato Monosodico)
Alcuni studi suggeriscono che il MSG può aumentare la risposta insulinica e contribuire all'insulino-resistenza, probabilmente attraverso l'overstimolazione dei neuroni ipotalamici che regolano l'appetito e il metabolismo.
Metalli Pesanti
- Arsenico (nell'acqua potabile): Associato a ridotta sensibilità insulinica
- Cadmio (fumo, alimenti contaminati): Danneggia le cellule beta pancreatiche
- Mercurio (pesce di grossa taglia): Interferisce con il metabolismo del glucosio
Una Nota Sul Sale
Paradossalmente, troppo poco sale può causare insulino-resistenza.
Quando restringi eccessivamente il sodio, il corpo attiva l'aldosterone (un ormone che ordina ai reni di trattenere sodio). L'aldosterone antagonizza l'insulina, creando resistenza.
La soluzione non è ovviamente abbuffarsi di sale, ma evitare restrizioni estreme (<2-3 g/die) se non medicamente necessarie.
CAUSA 5: Dieta (Oltre i Carboidrati)
Ora arriviamo alla parte che tutti pensano di conoscere: la dieta. Ma come vedrai, non è semplice come "taglia i carboidrati e guarisci".
Fruttosio: Il Carboidrato Speciale
Il fruttosio (presente nello zucchero da tavola, sciroppo di mais ad alto contenuto di fruttosio, frutta in eccesso) ha un metabolismo unico che lo rende particolarmente dannoso per il fegato.
Perché il fruttosio è diverso dal glucosio:
- Metabolizzato solo dal fegato: A differenza del glucosio (usato da tutti i tessuti), il fruttosio viene processato quasi esclusivamente dal fegato.
- Promuove la lipogenesi de novo: Il fruttosio viene convertito direttamente in grasso epatico attraverso un processo enzimatico che bypassa i normali meccanismi di regolazione.
- Non stimola insulina direttamente: Questo sembra un vantaggio, ma non lo è – significa che il fruttosio può essere consumato in grandi quantità senza attivare i segnali di sazietà.
Risultato:
- Steatosi epatica (fegato grasso)
- Aumento dei trigliceridi
- Aumento del grasso viscerale
- Insulino-resistenza epatica
Nota importante: Il fruttosio dalla frutta intera (con fibre, acqua, micronutrienti) è molto diverso dal fruttosio concentrato in bevande zuccherate o dolci. La dose fa il veleno.
Oli Vegetali Industriali e Acidi Grassi Omega-6
Gli oli vegetali industriali (mais, girasole, soia, canola) sono ricchi di acido linoleico (omega-6). Il problema non è l'omega-6 in sé, ma:
- Quantità eccessiva: La dieta moderna contiene 10-20 volte più omega-6 rispetto a 100 anni fa (rapporto omega-6:omega-3 di 20:1 invece di 2:1).
- Ossidazione: Gli omega-6 sono polinsaturi e altamente suscettibili all'ossidazione (soprattutto se riscaldati). L'ossidazione produce 4-HNE e altri aldeidi tossiche.
Come abbiamo visto prima:
- Il 4-HNE forza le cellule adipose a diventare ipertrofiche
- Causa stress ossidativo e infiammazione
- Induce insulino-resistenza
Soluzione pratica: Ridurre oli vegetali industriali e favorire:
- Olio extravergine d'oliva (omega-9, stabile)
- Burro/ghee da animali grass-fed
- Olio di cocco (grassi saturi a catena media)
Dolcificanti Artificiali
I dolcificanti artificiali (aspartame, sucralosio, saccarina) sono un tema controverso. La ricerca è mista:
Possibili meccanismi di danno:
- Alterazione del microbioma intestinale: Alcuni studi mostrano che i dolcificanti possono modificare la composizione batterica intestinale in modo sfavorevole
- Fase cefalica di secrezione insulinica: Il sapore dolce potrebbe stimolare un rilascio anticipato di insulina, anche senza glucosio
- Aumento dell'appetito: Potrebbero disregolare i segnali di sazietà
Evidenze contrastanti: Studi a breve termine in umani non mostrano effetti significativi sulla glicemia o insulina. Ma studi osservazionali a lungo termine associano l'uso di dolcificanti a maggior rischio di diabete (potrebbe essere confounding).
Conclusione neutrale: I dolcificanti artificiali probabilmente non sono il male assoluto, ma nemmeno completamente innocui. L'uso occasionale sembra sicuro; l'abuso cronico è da evitare.
CAUSA 6: Stile di Vita (Sedentarietà, Sonno, Luce)
 Le tue abitudini quotidiane hanno un impatto enorme sulla sensibilità insulinica – spesso più della dieta stessa.
Le tue abitudini quotidiane hanno un impatto enorme sulla sensibilità insulinica – spesso più della dieta stessa.
Sedentarietà: I Muscoli Che Non Lavorano Si "Chiudono"
I muscoli scheletrici sono il principale "lavandino" del glucosio, responsabili del 70% dello smaltimento post-prandiale. Ma solo se li usi.
Cosa succede quando sei sedentario:
- Dopo solo 3-5 giorni di inattività, i muscoli diventano significativamente più resistenti all'insulina
- I trasportatori GLUT4 si riducono
- La capacità ossidativa dei mitocondri diminuisce
- Gli acidi grassi si accumulano (lipidi intramiocellulari) → ceramidi → resistenza
La buona notizia: L'effetto è rapidamente reversibile. Una singola sessione di esercizio migliora la sensibilità insulinica per 24-48 ore. L'esercizio regolare mantiene i muscoli "affamati" di glucosio.
Il tipo di esercizio conta:
- Aerobico (cardio): Migliora l'uptake di glucosio durante l'esercizio
- Resistenza (pesi): Aumenta la massa muscolare (più "lavandini") e migliora la sensibilità a riposo
- HIIT: Effetto combinato potente su sensibilità insulinica
Sonno: La Privazione Che Ti Distrugge
La privazione cronica del sonno è uno dei fattori più sottovalutati e devastanti per la sensibilità insulinica.
Studi sperimentali mostrano:
- Una sola notte di sonno ridotto (4 ore) può ridurre la sensibilità insulinica del 20-30%
- Una settimana di sonno insufficiente (<6 ore/notte) può indurre uno stato pre-diabetico in giovani sani
Meccanismi:
- Aumento del cortisolo: La privazione del sonno aumenta il cortisolo (ormone antagonista dell'insulina)
- Alterazione della leptina e grelina:
- Leptina (sazietà) diminuisce
- Grelina (fame) aumenta
- Risultato: mangi di più, soprattutto carboidrati
- Attivazione del sistema nervoso simpatico: Più adrenalina → insulino-resistenza
- Riduzione della clearance del glucosio: Il metabolismo cerebrale del glucosio si altera
Quante ore servono? La maggior parte degli adulti ha bisogno di 7-9 ore di sonno di qualità. Meno di 6 ore cronicamente è un fattore di rischio metabolico significativo.
Luce Blu e Ritmi Circadiani
L'esposizione alla luce blu (schermi di computer, smartphone, TV) la sera sopprime la produzione di melatonina, l'ormone che regola il ciclo sonno-veglia.
Perché questo peggiora l'insulino-resistenza:
- Disregolazione circadiana: Il metabolismo del glucosio segue ritmi circadiani. La luce serale confonde l'orologio biologico.
- Soppressione della melatonina: La melatonina non regola solo il sonno – ha anche effetti diretti sulla sensibilità insulinica e sulla funzione delle cellule beta pancreatiche.
- Alterazione del cortisolo: Il cortisolo dovrebbe essere alto al mattino e basso la sera. La luce serale inverte questo pattern.
Soluzione pratica:
- Evitare schermi 2 ore prima di dormire
- Usare filtri luce blu o occhiali con lenti arancioni
- Dormire in una stanza completamente buia
Restrizione Calorica Estrema e Fame
Paradossalmente, la restrizione calorica estrema prolungata (diete crash, digiuno prolungato senza strategia) può peggiorare l'insulino-resistenza.
Meccanismo:
- Lo stress da fame aumenta il cortisolo
- Il corpo entra in "modalità risparmio energetico"
- La sensibilità insulinica può diminuire come meccanismo di conservazione
Differenza chiave:
- Digiuno intermittente ben strutturato (16:8, 18:6) = benefico
- Restrizione calorica cronica severa (<1000 kcal/die per mesi) = dannoso
CAUSA 7: Fattori Non Modificabili (Età, Genetica, Etnia)
Alcune cause dell'insulino-resistenza sono fuori dal tuo controllo. Conoscerle è importante per capire il tuo livello di rischio.
Età
L'invecchiamento è associato a:
- Perdita di massa muscolare (sarcopenia): Meno muscoli = meno capacità di smaltire glucosio
- Calo degli ormoni sessuali: Estrogeni e testosterone (protettivi) diminuiscono
- Accumulo di grasso viscerale: Con l'età, il grasso tende a redistribuirsi dall'area sottocutanea a quella viscerale
- Infiammazione cronica di basso grado (inflammaging): L'invecchiamento è accompagnato da un aumento basale di citochine infiammatorie
- Disfunzione mitocondriale: I mitocondri invecchiano e producono più ROS, meno ATP
Non puoi fermare l'età, ma puoi rallentarne gli effetti metabolici con esercizio di resistenza (preserva muscoli), dieta anti-infiammatoria, e controllo del peso.
Genetica
Alcune persone sono geneticamente predisposte all'insulino-resistenza attraverso varianti genetiche che influenzano:
- La funzione del recettore dell'insulina
- La capacità di espansione del tessuto adiposo (iperplasia vs ipertrofia)
- La distribuzione del grasso corporeo
- La funzione delle cellule beta pancreatiche
Geni coinvolti includono:
- TCF7L2: Varianti associate a diabete tipo 2
- FTO: Associato a obesità e distribuzione del grasso
- PPARG: Regola la differenziazione degli adipociti
Ma attenzione: La genetica predispone, non determina. L'ambiente (dieta, stile di vita) è il fattore scatenante. Come si dice: "La genetica carica la pistola, l'ambiente preme il grilletto."
Etnia
Alcune etnie hanno un rischio significativamente maggiore di insulino-resistenza e diabete tipo 2 rispetto ai caucasici, anche a parità di BMI:
Popolazioni ad alto rischio:
- Ispanici/Latino-Americani: Rischio 2-3 volte superiore
- Asiatici (Sud-Asiatici, Est-Asiatici):
- Sviluppano insulino-resistenza a BMI più bassi (es. 23-25 invece di 30)
- Maggior tendenza ad accumulare grasso viscerale
- Nativi Americani: Tra le popolazioni con il più alto tasso di diabete tipo 2 al mondo (alcune tribù >50%)
- Afro-Americani: Rischio aumentato, ma con pattern lipidico diverso (TG/HDL ratio meno predittivo)
Cause ipotizzate:
- Varianti genetiche specifiche
- "Thrifty genotype" hypothesis: geni adattati a periodi di carestia (risparmio energetico) diventano svantaggiosi in abbondanza alimentare
- Differenze nella distribuzione del grasso corporeo
Implicazione pratica: Se appartieni a un'etnia ad alto rischio, devi essere ancora più proattivo nella prevenzione.
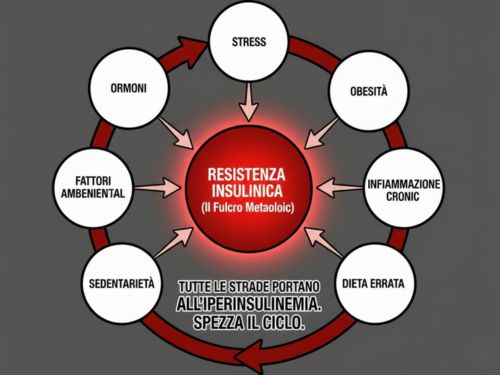
La Causa Unica Che Unifica Tutto: Iperinsulinemia
Torniamo al punto di partenza. Abbiamo visto 7 categorie di cause, decine di meccanismi diversi. Ma c'è un denominatore comune che emerge da tutti:
Tutte le strade portano all'iperinsulinemia cronica.
- Stress → Cortisolo → Glicemia alta → Iperinsulinemia compensatoria
- Obesità → Resistenza → Iperinsulinemia compensatoria
- Infiammazione → Resistenza → Iperinsulinemia compensatoria
- Carboidrati raffinati → Picchi glicemici → Iperinsulinemia
- Sedentarietà → Resistenza muscolare → Iperinsulinemia compensatoria
E l'iperinsulinemia stessa, come abbiamo visto, è la causa principale di ulteriore resistenza.
Questo è il motivo per cui la strategia terapeutica fondamentale è abbassare l'insulina.
Non importa quale combinazione di cause ti ha portato qui. Una volta che l'iperinsulinemia cronica si stabilisce, diventa il motore centrale della malattia.
E se l'insulina è il problema centrale, la soluzione è chiara: dobbiamo spezzare il circolo vizioso abbassando i livelli di insulina e ripristinando la sensibilità cellulare.
Compila il modulo qui sotto per fissare una consulenza.
