Diabete Tipo 1 vs Diabete Tipo 2: Le principali differenze e il ruolo dell’alimentazione
Per comprendere il diabete e soprattutto per capire perché l’alimentazione rappresenti il fulcro della gestione clinica, indipendentemente dalla tipologia, è necessario fare un passo indietro e smontare una delle più grandi semplificazioni della medicina moderna: l’idea che “il diabete sia una sola malattia”.
Il diabete di Tipo 1 e il diabete di Tipo 2 condividono lo stesso segno clinico finale, l’iperglicemia, ma nascono da meccanismi fisiopatologici opposti.
Comprendere questa distinzione non è un esercizio accademico: è la base per evitare errori terapeutici, per spiegare perché molte strategie falliscono nel lungo periodo e per comprendere come un approccio alimentare corretto possa rappresentare un denominatore comune efficace, pur in contesti clinici molto diversi.
Il diabete non è una malattia unica, ma un insieme di disordini metabolici
 Il termine diabete mellito non identifica una singola patologia, ma una famiglia di disturbi metabolici accomunati dall’incapacità dell’organismo di mantenere la glicemia entro un range fisiologico. Esistono forme secondarie (farmaco-indotte, genetiche rare, legate a patologie pancreatiche) e il diabete gestazionale, ma nella pratica clinica oltre il 95% dei casi rientra in due categorie principali:
Il termine diabete mellito non identifica una singola patologia, ma una famiglia di disturbi metabolici accomunati dall’incapacità dell’organismo di mantenere la glicemia entro un range fisiologico. Esistono forme secondarie (farmaco-indotte, genetiche rare, legate a patologie pancreatiche) e il diabete gestazionale, ma nella pratica clinica oltre il 95% dei casi rientra in due categorie principali:
- Diabete di Tipo 2, che rappresenta circa il 90–95% di tutti i casi a livello globale.
- Diabete di Tipo 1, molto meno frequente ma in costante aumento di incidenza.
Il problema nasce quando queste due condizioni vengono messe nello stesso calderone, trattate come se fossero varianti quantitative dello stesso disturbo, anziché entità qualitativamente differenti. Questo errore concettuale ha conseguenze enormi, soprattutto sul piano terapeutico.
Due cause opposte, stesso risultato finale: l’iperglicemia
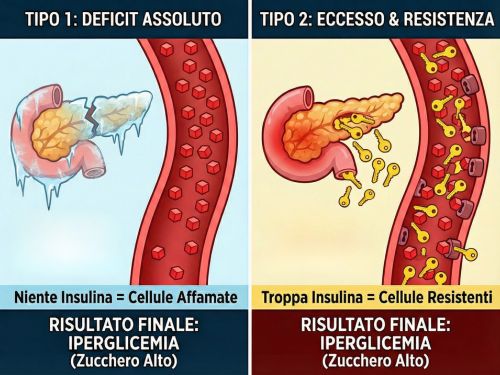
Il dato apparentemente paradossale è che due malattie opposte producono lo stesso esito clinico: zucchero alto nel sangue. Ma il perché la glicemia salga è radicalmente diverso.
L’iperglicemia non è la malattia: è il segnale, il campanello d’allarme. Concentrarsi solo su quel numero significa trattare il termometro e ignorare l’infezione.
Diabete di Tipo 1: una malattia da deficit assoluto di insulina
Il diabete di Tipo 1 è, a tutti gli effetti, una malattia autoimmune.
Il sistema immunitario, per ragioni non ancora completamente chiarite, riconosce come “nemiche” le cellule beta del pancreas, responsabili della produzione di insulina, e le distrugge progressivamente. Il risultato è una carenza assoluta di insulina.
Cosa significa, in termini pratici?
L’insulina non è un “farmaco per abbassare la glicemia”, ma un ormone anabolico essenziale alla vita. È il segnale che permette al glucosio di entrare nelle cellule per essere utilizzato come carburante.
Nel diabete di Tipo 1:
- Il glucosio rimane nel sangue.
- Le cellule restano energeticamente affamate.
- Il corpo entra in uno stato di catabolismo estremo.
È per questo che il paziente:
- Mangia molto ma dimagrisce rapidamente.
- Sviluppa chetosi patologica fino alla chetoacidosi diabetica, una condizione potenzialmente letale.
Dal punto di vista laboratoristico, nel sangue sono spesso presenti autoanticorpi diretti contro le isole pancreatiche, a conferma dell’origine autoimmune del processo.
Qui non esistono scorciatoie terapeutiche
Nel diabete di Tipo 1, l’insulina è una terapia salvavita. Non è un’opzione, non è negoziabile. Senza insulina esogena, il metabolismo collassa.
Questo punto è fondamentale per evitare fraintendimenti: nessun approccio alimentare “cura” il diabete di Tipo 1 nel senso di eliminarne la causa. Tuttavia, e questo sarà centrale più avanti, l’alimentazione determina quanta insulina è necessaria, quanto è stabile la glicemia e quante complicanze si accumulano nel tempo.
Diabete di Tipo 2: una malattia da eccesso di insulina
Il diabete di Tipo 2 è l’esatto opposto fisiologico. Qui il problema non è la mancanza di insulina, ma il fatto che ce n’è già troppa.
La resistenza insulinica è il vero cuore del problema.
Nel diabete di Tipo 2:
- Le cellule diventano progressivamente resistenti al segnale insulinico.
- Il pancreas risponde producendo sempre più insulina per forzare l’ingresso del glucosio.
- Si instaura uno stato cronico di iperinsulinemia compensatoria.
Per anni, spesso decenni, la glicemia può rimanere “normale” proprio grazie a questi livelli elevati di insulina. È per questo che il diabete di Tipo 2 non nasce all’improvviso.
Il percorso tipico è:
- Normoglicemia con iperinsulinemia
- Insulino-resistenza
- Prediabete
- Diabete conclamato
Quando la glicemia finalmente sale, il danno metabolico è già avanzato.
Diabete di tipo 1 e Diabete di tipo 2: Due profili clinici profondamente diversi
Età di esordio e contesto clinico
Il diabete di Tipo 1:
- Compare spesso in infanzia o adolescenza
- Può comunque manifestarsi a qualsiasi età
- Non è legato all’obesità
- È frequentemente associato ad altre patologie autoimmuni (tiroidite, vitiligine, morbo di Graves)
Il diabete di Tipo 2:
- Era storicamente una malattia dell’adulto
- Oggi è sempre più frequente anche in età pediatrica
- È fortemente associato a:
- Sovrappeso e obesità
- Sindrome metabolica
- Sedentarietà
- Alimentazione iperinsulinizzante cronica
Sintomi: acuto vs silenzioso
Il Tipo 1 si presenta spesso in modo drammatico:
- Sete intensa
- Poliuria
- Fame e perdita di peso
- Stanchezza estrema
- Rischio di chetoacidosi
Il Tipo 2, al contrario, è subdolo:
- Può restare asintomatico per anni
- Viene diagnosticato per caso
- Quando compaiono i sintomi, le complicanze sono spesso già presenti
Diabete di tipo 1 e Diabete di tipo 2: Il grande paradosso terapeutico

Due malattie:
- Una da deficit insulinico
- Una da eccesso insulinico
Vengono spesso trattate con la stessa strategia farmacologica: aumentare l’insulina.
Nel Tipo 1 è corretto.
Nel Tipo 2 è un errore concettuale.
Questo non significa che l’insulina non abbia un ruolo nel Tipo 2 in determinate fasi cliniche. Significa che non può essere la soluzione di base, perché non affronta la causa.
Approfondimento: Il ruolo dell'alimentazione nel Diabete di Tipo 1 e di Tipo 2
Nonostante le differenze fisiopatologiche radicali tra diabete di Tipo 1 e Tipo 2, la riduzione del carico glucidico rappresenta un intervento trasversale efficace, supportato da evidenze scientifiche consistenti. Il razionale è semplice ma potente: meno carboidrati ingeriti significano meno glucosio da gestire, con benefici che si manifestano attraverso meccanismi differenti ma convergenti verso lo stesso risultato clinico.
Nel diabete di Tipo 1, dove l'insulina manca, ridurre i carboidrati significa ridurre proporzionalmente la dose di insulina esogena necessaria. Nel diabete di Tipo 2, dove l'insulina è cronicamente elevata, la restrizione carboidratica riduce lo stimolo iperinsulinizzante che alimenta la resistenza insulinica, riuscendo quindi a ridurre se non addirittura a eliminare i farmaci. Due problemi opposti, una soluzione comune.
Diabete di Tipo 1: oltre la conta dei carboidrati
La gestione alimentare tradizionale del diabete di Tipo 1 si basa sulla conta dei carboidrati (CHO counting), strategia che permette di adattare la dose di insulina alla quantità di carboidrati assunti nel pasto. Questo approccio funziona, ma ha un limite intrinseco: più carboidrati si assumono, più insulina serve, e più diventa difficile evitare errori nel dosaggio che portano a ipoglicemie o iperglicemie.
La ricerca più recente ha dimostrato che ridurre drasticamente l'intake di carboidrati può migliorare significativamente la stabilità glicemica. Una meta-analisi pubblicata su eClinicalMedicine nel 2025 (approfondisci qui), che ha valutato 35 studi randomizzati controllati, ha evidenziato come le diete a ridotto contenuto di carboidrati (≤45% delle calorie totali) migliorano significativamente il tempo in range glicemico (+3,84%), riducono la variabilità glicemica (-3,24%) e diminuiscono il fabbisogno insulinico giornaliero di 5,63 unità in media.
Un'altra meta-analisi del 2025 pubblicata su Nutrients (Approfondisci qui) ha confermato che le diete low-carb nel diabete di Tipo 1 riducono in particolare l'insulina ai pasti (bolo) di 8,61 unità al giorno, senza effetti negativi significativi sull'emoglobina glicata. La riduzione del fabbisogno insulinico non è un dettaglio secondario: meno insulina significa meno margine di errore, meno rischio di ipoglicemie severe e, nel lungo periodo, minore esposizione all'"iperinsulinemia iatrogena" che l'insulina esogena può causare.
Un case report interessantissimo (approfondisci qui) pubblicato nel 2024 sul Journal of Clinical Endocrinology & Metabolism descrive un paziente con diabete di Tipo 1 che ha seguito una dieta chetogenica (≤50g di carboidrati al giorno) per 10 anni consecutivi. I risultati sono stati straordinari: l'emoglobina glicata è scesa dal 6,8% al 5,5% (un valore quasi normoglicemico), il fabbisogno insulinico si è ridotto del 43%, e il tempo in range glicemico ha raggiunto il 90%, il tutto senza episodi di ipoglicemia grave o chetoacidosi diabetica in un decennio. Questi dati dimostrano che una restrizione carboidratica sostenuta e ben gestita può portare a un controllo metabolico eccezionale, difficilmente raggiungibile con approcci convenzionali.
È importante sottolineare che nel diabete di Tipo 1 la dieta a basso contenuto di carboidrati non "cura" la malattia, ma ottimizza la gestione riducendo la complessità del problema: meno glucosio da controllare, meno insulina necessaria, meno variabilità, meno complicanze. Ed è fondamentale sottolineare che approcci chetogenici non sono ancora la prassi, ma nuove frontiere che verranno presto sperimentate e adattate anche per il diabete tipo 1.
Diabete di Tipo 2: spegnere l'iperinsulinemia cronica
Nel diabete di Tipo 2, l'approccio alimentare ha un potenziale ancora più trasformativo perché può agire direttamente sulla causa della malattia: l'eccesso di insulina e la resistenza insulinica. Qui il meccanismo d'azione è completamente diverso rispetto al Tipo 1, ma altrettanto efficace.
Numerose meta-analisi pubblicate tra il 2020 e il 2025 hanno consolidato le evidenze sull'efficacia delle diete a ridotto contenuto di carboidrati. Una meta-analisi pubblicata su Nutrition & Diabetes nel 2020 (approfondisci qui) , che ha incluso 14 studi randomizzati controllati con 734 partecipanti, ha dimostrato che la dieta chetogenica riduce significativamente l'emoglobina glicata (-1,07%), la glicemia a digiuno (-1,29 mmol/L), i trigliceridi (-0,72 mmol/L) e migliora la sensibilità insulinica, con effetti più marcati nei pazienti con obesità.
Una revisione sistematica del 2022 su Diabetes, Obesity and Metabolism (approfondisci qui), che ha analizzato 8 studi con 606 partecipanti, ha confermato che le diete chetogeniche nel diabete di Tipo 2 migliorano il controllo glicemico e riducono significativamente il peso corporeo nei primi 6 mesi, con effetti superiori rispetto alle diete raccomandate standard.
Il digiuno intermittente, che rappresenta un'estensione logica della restrizione carboidratica, ha anch'esso dimostrato efficacia. Una meta-analisi pubblicata nel 2025 su Diabetes & Metabolic Syndrome (approfondisci qui ), che ha incluso 17 studi con 1.169 partecipanti, ha evidenziato un miglioramento significativo del controllo glicemico, con effetti particolarmente marcati nei pazienti con BMI elevato e alta aderenza al protocollo. L'analisi ha mostrato che il time-restricted eating (alimentazione in finestra temporale ristretta) produce i migliori risultati in termini di riduzione dell'emoglobina glicata e della glicemia a digiuno.
I meccanismi biochimici: dal fegato alle cellule
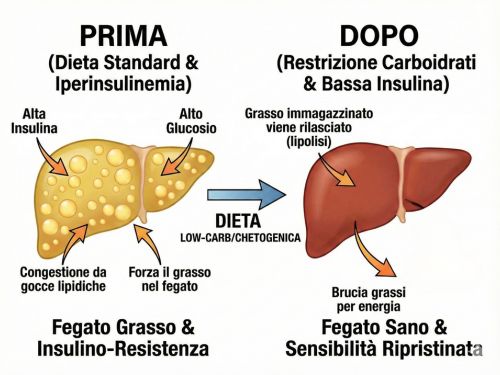 Per comprendere perché la restrizione carboidratica funzioni così bene nel diabete di Tipo 2, è necessario guardare a ciò che accade a livello epatico e cellulare.
Per comprendere perché la restrizione carboidratica funzioni così bene nel diabete di Tipo 2, è necessario guardare a ciò che accade a livello epatico e cellulare.
Il fegato grasso (steatosi epatica) non è solo una conseguenza del diabete di Tipo 2, ma un attore centrale nella progressione della resistenza insulinica. Quando il fegato accumula grasso, si genera un circolo vizioso: l'accumulo di diacilglicerolo (DAG) attiva la protein chinasi C epsilon (PKCε), che interferisce con la segnalazione insulinica epatica, perpetuando l'insulino-resistenza e aumentando la produzione epatica di glucosio (gluconeogenesi).
La riduzione dell'intake di carboidrati interrompe questo circolo vizioso attraverso più meccanismi:
- Riduzione della lipogenesi de novo: meno carboidrati significano meno glucosio disponibile per essere convertito in grasso epatico. Uno studio pubblicato nel 2025 sul Journal of Clinical Endocrinology & Metabolism (approfondisci qui) ha dimostrato che una dieta chetogenica riduce in maniera significativa il quantitativo di grasso epatico.
- Riduzione dell'iperinsulinemia: l'insulina cronicamente elevata stimola l'accumulo di grasso epatico. Abbassando l'insulina circolante attraverso la riduzione dei carboidrati, si favorisce la lipolisi del grasso epatico e l'ossidazione degli acidi grassi, riducendo così il contenuto lipidico del fegato.
- Miglioramento della sensibilità insulinica muscolare: la restrizione carboidratica migliora l'uptake di glucosio da parte del muscolo scheletrico, riducendo il dirottamento del glucosio verso il fegato dove verrebbe convertito in grasso. L'esercizio fisico è in grado di ridurre la lipogenesi epatica post-prandiale aumentando la sintesi di glicogeno muscolare.
- Riduzione della gluconeogenesi: la diminuzione del grasso epatico si associa a una riduzione della produzione endogena di glucosio.
Dalla teoria alla pratica clinica
I dati convergono verso una conclusione chiara: la restrizione carboidratica, nelle sue varie forme (dieta low-carb moderata, dieta chetogenica, digiuno intermittente), rappresenta uno strumento terapeutico potente sia nel diabete di Tipo 1 che nel Tipo 2, pur attraverso meccanismi diversi.
Nel Tipo 1, l'obiettivo è minimizzare la complessità e migliorare la sensibilità insulinica (migliore risposta al farmaco): meno carboidrati da gestire significa meno insulina da dosare, meno variabilità glicemica, meno errori, meno ipoglicemie. È un approccio che semplifica il problema senza eliminarlo.
Nel Tipo 2, l'obiettivo è affrontare la causa: ridurre lo stimolo insulinico cronico, svuotare il fegato dal grasso accumulato, ripristinare la sensibilità insulinica. È un approccio che può portare alla remissione della malattia, non solo al suo controllo.
In entrambi i casi, l'alimentazione non è "un contorno" della terapia, ma la leva primaria su cui costruire risultati duraturi. I farmaci possono tamponare, ma solo l'intervento alimentare può modificare il terreno metabolico di base. Ed è per questo che il focus principale di qualsiasi strategia terapeutica dovrebbe sempre partire da ciò che entra dalla bocca, prima ancora di pensare a ciò che si inietta o si prescrive.
Punto chiave da portare a casa
Il diabete di Tipo 1 e il diabete di Tipo 2 non sono la stessa malattia, non sono “gradi diversi” dello stesso problema e non dovrebbero essere trattati allo stesso modo.
Ma esiste un terreno comune: controllare ciò che entra nel sangue prima ancora di cercare di correggere ciò che c’è già.
Ed è da qui che inizia tutto il resto del ragionamento: perché la glicemia sale, perché il problema non è solo lo zucchero, e perché continuare a “tamponare” senza spegnere l’incendio metabolico è una strategia destinata a fallire.
